Les organoïdes répliquent nos organes en laboratoire
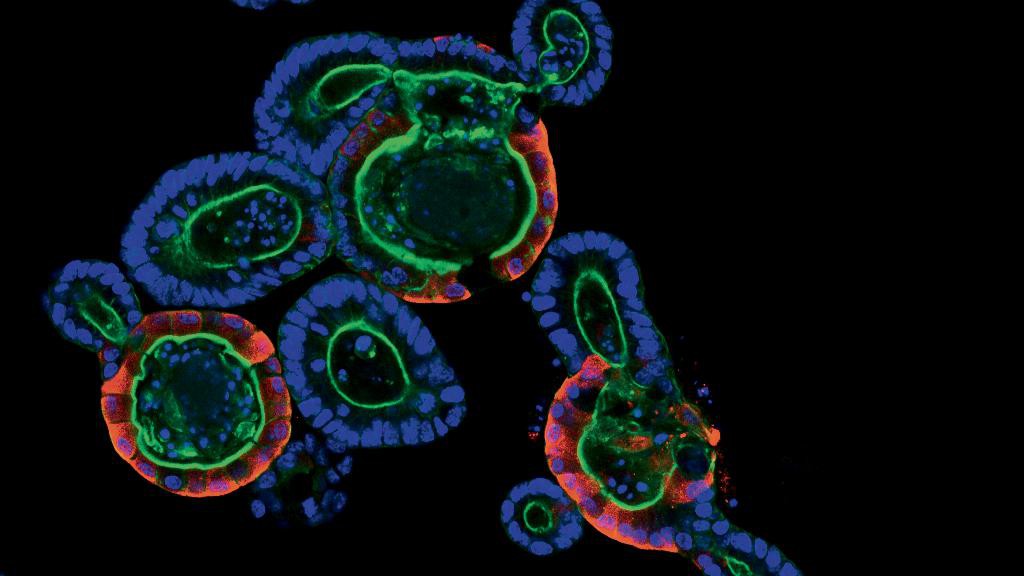
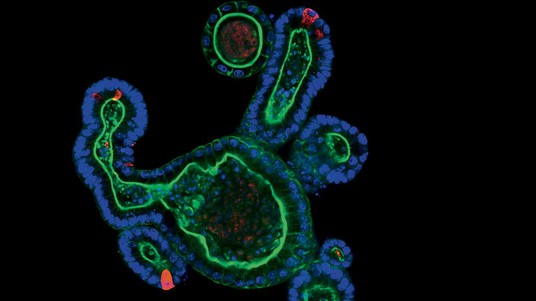
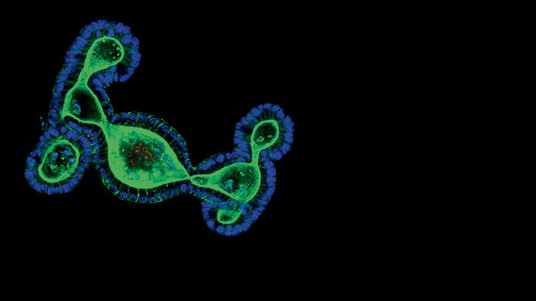
Organoïdes intestinaux cultivés dans des hydrogels synthétiques. © Saba Rezakhani, Lütolf lab/EPFL
DOSSIER ORGANOÏDES 1/3 – Des organes miniatures, pas plus grands qu’un grain de poivre, transforment depuis 10 ans la recherche autour des cellules souches et rapprochent, du même coup, l’in vitro de l’in vivo. Ils ouvrent des perspectives inédites vers la médecine personnalisée, le traitement des cancers et la modélisation des maladies. L’EPFL vient de s’associer au CHUV pour une nouvelle étude alors que cette technologie a déjà permis la naissance de plusieurs start-ups sur le campus.
Le coup de tonnerre qui a fait trembler les biologistes est arrivé il y a à peine 10 ans. En 2009, le laboratoire de Hans Clevers, de l'Hubrecht Institut aux Pays-Bas, publie un important papier qui montre, pour la première fois, un organoïde d’intestin. «C’était un choc pour beaucoup de biologistes, se souvient Matthias Lütolf, dont le laboratoire est spécialisé dans la biologie et bioingénierie des cellules souches à l’EPFL. Cette découverte allait à l’encontre du dogme qui voulait qu’une cellule, pour devenir un tissu, ait besoin d’être dans le contexte d’un organisme, de communiquer avec de nombreux autres types de cellules.» Ce travail a montré de manière très claire que les cellules-souches peuvent s’organiser et adopter les fonctionnalités des tissus et des organes si on les cultive dans un milieu tridimensionnel adapté. Pionnière, l’Europe reste aujourd’hui encore à la tête de la recherche dans ce domaine. Et l’EPFL bénéficie d’un environnement particulièrement riche en ingénierie, des atouts qui attirent des biologistes du monde entier désireux d'améliorer cette technologie.
Une médecine personnalisée
Grâce aux organoïdes, le fossé entre l’in vitro et l’in vivo a été réduit significativement. Ces cultures cellulaires en 3 dimensions, plus réalistes, ont ouvert de nombreux champs d’exploration dans la pose de diagnostics, la recherche de médicaments ou la modélisation des maladies, voire même pour remplacer des tissus endommagés. La médecine personnalisée pourra aussi en bénéficier, notamment dans le combat contre le cancer. Un organoïde a, en effet, la faculté d’exprimer les mêmes mutations que les cellules originelles prélevées sur le tissu malade d’un patient. Il va reproduire l’anomalie spécifique et génétiquement unique d’une personne. Une collaboration entre l’EPFL et le département d’oncologie du CHUV vient de débuter et se poursuivra sur trois ans avec pour objectif de développer des outils pour la prédiction des réponses aux traitements oncologiques. «Dans la culture ex vivo les organoïdes se développent sans être parfaitement conformes aux cellules dans l’être humain, explique le docteur Krisztian Homicsko, pour cela il faut optimiser les cultures dans lesquelles les cellules grandissent. Le laboratoire de Matthias Lütolf nous permet pour la première fois d’analyser et de comparer nos échantillons avec leurs organoïdes.» L’idée est tellement réjouissante que le monde médical a commencé à créer des banques d’organoïdes pour tester les médicaments comme on le ferait dans des essais cliniques.
Ethique et expérimentation
Et l’éthique dans la culture cellulaire ? Le journal Nature a consacré deux pages à la question. Surtout si l’on considère que ces organoïdes peuvent devenir des microcœurs ou microcerveaux avec toutes les caractéristiques du tissu cérébral embryonnaire. Savoir capturer les caractéristiques physiologiques d’un cerveau humain permettra-t-il de surveiller une personne ? Autre question importante, aura-t-on encore besoin de l’expérimentation animale ? «Une culture de cellules est bien loin d’un essai sur un être vivant, il ne faut pas rêver. Les organoïdes peuvent réduire l’expérimentation animale, mais pas la supprimer complètement. Tous les sujets de recherche ne pourront pas être étudiés sur des organoïdes et il faudra de toute façon toujours vérifier les résultats sur un animal», précise Denis Duboule, dont le domaine de prédilection est l’embryologie, la génétique et la génomique du développement des mammifères. Son laboratoire a même réussi à recréer des organoïdes d’embryon précoce.
Comme la médecine génomique en son temps, les organoïdes sont en passe de devenir un outil qui permettra de répondre à de nombreuses questions posées par la science.

Les organoïdes, des micro-organes
Cerveau, thyroïde, thymus, intestin, foie, pancréas, estomac, poumons, reins, embryons précoces, les chercheurs cultivent de nombreux organoïdes, version miniature de nos organes. Mais comment font-ils ?
Nos organes sont constitués de différents types cellulaires organisés en couches ou en réseaux. Il ne suffit pas de poser des cellules-souches dans une boîte de Petri pour voir croître un organoïde. Il a fallu identifier, décoder et comprendre les signaux moléculaires, qui permettent la différenciation des cellules-souches dans l’embryon et des tissus adultes, pour donner naissance à des tissus tridimensionnels. C’est dans un environnement comprenant différents cocktails de signaux et un bon système de culture tridimensionnel, proche des conditions physiologiques, que les cellules-souches peuvent s’organiser et reproduire ce qu’elles font naturellement pendant l’embryogenèse ; adopter les fonctionnalités des tissus et construire des ébauches d’organes. Ces organoïdes, qui typiquement mesurent environ 300-500 microns (0,3-0,5 millimètre) peuvent également être obtenus non pas à partir de cellules-souches, mais, indirectement, de cellules adultes différenciées, des cellules qui sont déjà programmées dans un organe. Les scientifiques ont réussi à les rendre «pluripotentes», c’est-à-dire capables de se différencier en n'importe quel type de cellules de l'organisme. Avec les organoïdes, la recherche peut sonder de nouvelles voies de compréhension de la croissance de nos organes ex vivo.
Retrouvez l'ensemble des articles du dossier consacré aux organoïdes :
1 - Les organoïdes répliquent nos organes en laboratoire
2 - Un organoïde, pour quoi faire ?
3 - Organoïdes: Des savoir-faire valorisés par des start-ups