Une protéine modifiée booste les cellules anti-cancéreuses

Yu-Qing Xie, Ping-Chic Ho, Li Tang et Yugang Guo © Alain Herzog / 2021 EPFL
Des scientifiques de l’EPFL ont découvert que l’interleukin-10-Fc de fusion, une protéine modifiée, peut renforcer l’efficacité des lymphocytes T épuisés, ces cellules immunitaires capables de combattre le cancer, en reprogrammant leur métabolisme.
Contre le cancer, il existe plusieurs traitements, dont l’immunothérapie. Son principe est simple : le système immunitaire du patient, composé de lymphocytes ou cellules T, est stimulé afin que ces cellules T détruisent les cellules cancéreuses. Sans l’immunothérapie les lymphocytes restent inactifs face à la tumeur. Malgré son efficacité approuvée, ce traitement possède un défaut majeur : il ne fonctionne que sur 20 à 30% des patients. Une majorité de patients atteints de cancer ne peuvent bénéficier des immunothérapies actuelles.
Un travail d’équipe
Les scientifiques s’efforcent par tous les moyens d’augmenter ce ratio. À la faculté des sciences et techniques de l’ingénieur, le professeur Li Tang et son équipe du laboratoire de biomatériaux pour l’immunoingénierie ont collaboré avec des chercheurs de six autres laboratoires de différentes universités pour trouver un moyen de rendre l’immunothérapie plus efficace. En tout ce sont près de vingt-deux chercheurs qui ont allié leurs compétences en biologie, immunologie, bioingénierie, bioinformatique, entre autres. Leur étude est publiée dans Nature Immunology.

Booster les cellules T fatiguées
« Le fait qu’une majorité de patients ne réagissent pas à ce traitement reste un défi à relever. Une des explications est que les lymphocytes infiltrant la tumeur et luttant contre les cellules cancéreuses, s’épuisent et finissent par être incapables de contrôler la progression des cellules cancéreuses. Dans le jargon scientifique, nous disons que les cellules T dysfonctionnent. Elles ne répondent pas ou plus à l’immunothérapie », indique Li Tang.
Les chercheurs ont alors ajouté une protéine fabriquée artificiellement, nommée protéine de fusion interleukin-10-Fc, au traitement d’immunothérapie. « L'interleukin-10 peut soit stimuler, soit désactiver notre système immunitaire. Cependant, nous ne savions que peu de choses sur la manière exacte dont elle interagit avec les cellules T qui infiltrent la tumeur jusqu’à nos expériences, précise Yuqing Xie, assistant-doctorant. Mais, il semble que nous avons trouvé un nouveau mécanisme qui pourrait revitaliser les cellules T épuisées. » Les tests ont révélé que l’interleukin-10-Fc agit comme un booster d’énergie, permettant aux lymphocytes d’être réactivés et de continuer à combattre la tumeur. « En utilisant cette protéine, nous avons pu reprogrammer le métabolisme des cellules T et améliorer leurs rôles destructeurs de cancer ainsi que leur développement », ajoute Yugang Guo, doctorant.

LBI/Xiaomeng Hu/2021 EPFL
Plus de 90 % de guérison
Cette nouvelle immunothérapie a été testée sur des souris, et les résultats sont sans appel : plus de 90 % d’entre elles ont vaincu le cancer. « L’interleukin-10-Fc s’avère sûre et très efficace. Cette protéine entre en synergie avec l’immunothérapie par transfert de cellules T adoptives, comme la thérapie CAR-T, ou les inhibiteurs de points de contrôle immunitaires, conduisant à l’éradication de tumeurs et à des guérisons durables chez une majorité de souris soignées. Notre méthode semble améliorer considérablement les immunothérapies existantes contre les tumeurs solides, connues pour être difficiles à guérir », se réjouit Li Tang. D’après ces premiers tests, aucun effet secondaire n’a été observé, ce qui rend prometteurs les futurs essais cliniques. Les chercheurs Yugang Guo, Yuqing Xie et Li Tang ont déposé des brevets internationaux pour cette nouvelle thérapie et vont prochainement procéder à des essais cliniques sur des patients.
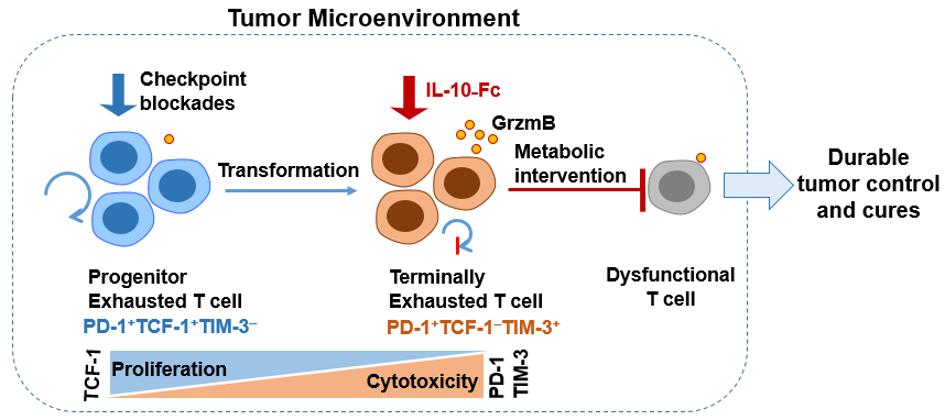
Percée du goulot d'étranglement
Parmi les cellules T infiltrant les tumeurs, un sous-ensemble appelé cellules T CD8+ en phase terminale, ne répond pas à la plupart des immunothérapies existantes, y compris les blocages des points de contrôle immunitaires. Il est connu pour être extrêmement difficile à réactiver. La recherche du professeur Li Tang montre que la reprogrammation métabolique de ces cellules par le biais d'une molécule, appelée transporteur de pyruvate mitochondrial, est suffisante pour restaurer la fonctionnalité des cellules T CD8+ épuisées en phase terminale dans la lutte contre le cancer. Cette découverte jette les bases d'une identification plus poussée des stimulations métaboliques nécessaires pour revigorer les cellules T CD8+ en phase terminale, un goulot d'étranglement majeur dans le domaine de l'immunothérapie du cancer.
This work was supported in part by the Swiss National Science Foundation (SNSF Project grant 315230_173243), ISREC Foundation with a donation from the Biltema Foundation, Swiss Cancer League (No. KFS-4600-08-2018), the European Research Council under the ERC grant agreement MechanoIMM (805337), Kristian Gerhard Jebsen Foundation, Fondation Pierre Mercier pour la science, Anna Fuller Fund grant, and EPFL (L.T.). P.-C.H. was supported in part by the Swiss Institute for Experiment Cancer Research (ISREC 26075483), the SNSF project grants (31003A_163204 and 31003A_182470), the Cancer Research Institute Lloyd J. Old STAR award, and European Research Council Staring Grant (802773-MitoGuide). P. R. was supported in part by grants from the SNSF (310030_182735 and 310030E-164187). W.H. was supported in part by the Swiss Cancer League (KFS-4407-02-2018) and the SNSF (310030B_179570). W.X. was supported in part by Strategic Priority Research Program of the Chinese Academy of Sciences (XDB29030000) and the Ministry of Science and Technology of China (2016YFC1303503). M.G. was supported by the Chinese Scholarship Council (CSC, No. 201808320453).
Guo, Y.#; Xie, Y.-Q.#; Gao, M.; Zhao, Y.; Franco, F.; Wenes, M.; Siddiqui, I.; Bevilacqua, A.; Wang, H.; Yang, H.; Feng, B.; Xie, X.; Sabatel, C.M.; Tschumi, B.; Chaiboonchoe, A.; Wang, Y.; Li, W.; Xiao, W.; Held, W.; Romero, P.; Ho, P.-C.*; Tang, L.* "Metabolic Reprogramming of Terminally Exhausted CD8+ T cells by IL-10 Enhances Anti-Tumor Immunity", Nat. Immunol. 2021, in press. DOI: 10.1038/s41590-021-00940-2