Un gène-clé derrière le lymphome folliculaire
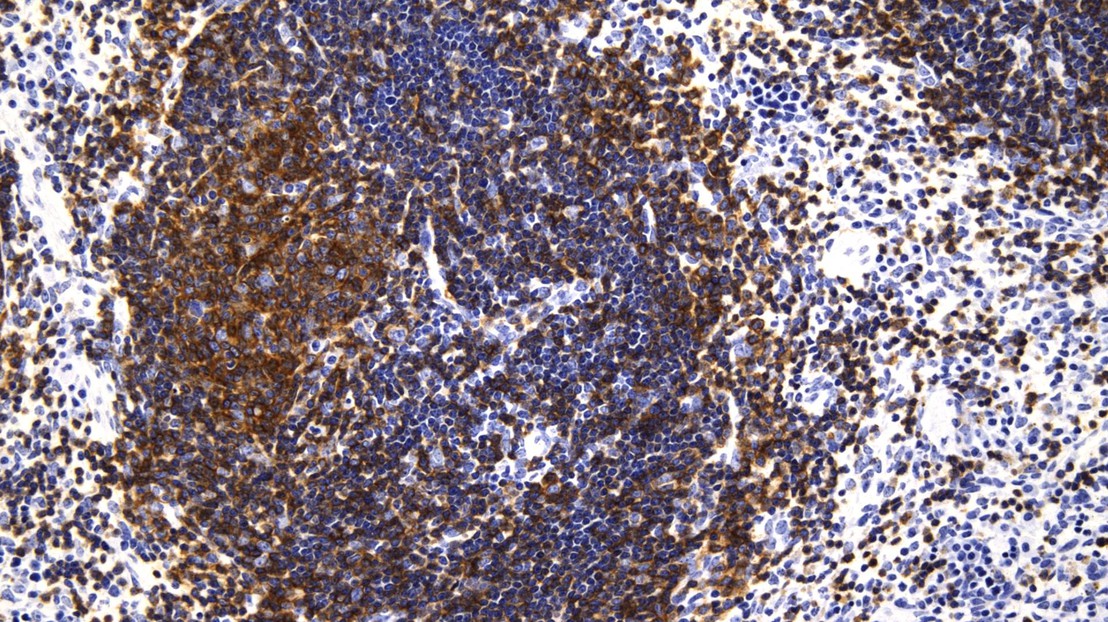
Expansion et accumulation de cellules de lymphome (colorées en brun) dans la rate de souris. Crédit: Natalya Katanayeva (EPFL)
Des scientifiques de l'EPFL ont découvert un gène important dont la perte est liée au développement du lymphome folliculaire, un cancer incurable.
Le lymphome folliculaire est un cancer incurable qui affecte plus de 200'000 personnes chaque année dans le monde. Il se développe lorsque l'organisme se met à créer des lymphocytes B anormaux, les lymphocytes B étant les globules blancs qui, dans des conditions normales, combattent les infections. Ce cancer est associé à plusieurs altérations de l'ADN de la cellule, mais jusqu'ici la question de savoir quel gène – ou gènes – est impliqué n'était pas claire. Des scientifiques de l'EPFL viennent d'analyser le génome de plus de 200 patients affectés d'un lymphome folliculaire, et ils ont découvert qu'un gène, Sestrine1, est fréquemment absent, ou dysfonctionnel, chez ces patients. Cette découverte ouvre la voie à de nouvelles options de traitement, et vient d'être publiée dans Science Translational Medicine.
L'une des caractéristiques courantes du lymphome folliculaire est une anomalie génétique entre deux chromosomes (14 et 18). Lorsque se produit un événement connu sous le nom de «translocation chromosomique», les deux chromosomes échangent certaines parties entre eux. Cela déclenche l'activation d'un gène qui empêche les cellules de mourir, rendant les cellules virtuellement immortelles – le trait distinctif d'une tumeur.
De plus, environ 30% des patients atteints de lymphome folliculaire perdent également une partie du chromosome 6, ce qui affecte de multiples gènes dont le rôle est d'empêcher l'émergence d'une tumeur. Ces patients ont généralement un pronostic défavorable. Un autre groupe, 20% des patients, présente des altérations qui provoquent une désorganisation chromosomique, et le dysfonctionnement consécutif de plusieurs gènes et protéines. Ce qu'il faut retenir, c'est que pour les deux groupes de patients, il est très difficile de repérer lesquels, parmi tous les gènes affectés, provoquent clairement la maladie.
Le laboratoire d'Elisa Oricchio à l'EPFL, en collaboration avec des collègues du Canada et des Etats-Unis, a analysé le génome de plus de 200 patients atteint de lymphome folliculaire. Les analyses ont révélé qu'un gène spécifique, Sestrine1, peut être endommagé à la fois par la perte du chromosome 6, et son extinction chez les patients.
Sestrine1 aide la cellule à se défendre contre les dommages à l'ADN – par exemple après une exposition à des radiations – et contre le stress oxydatif. En fait, Sestrine1 fait partie du mécanisme anti-tumeurs de la cellule, qui bloque la croissance de cellules potentiellement cancérigènes.
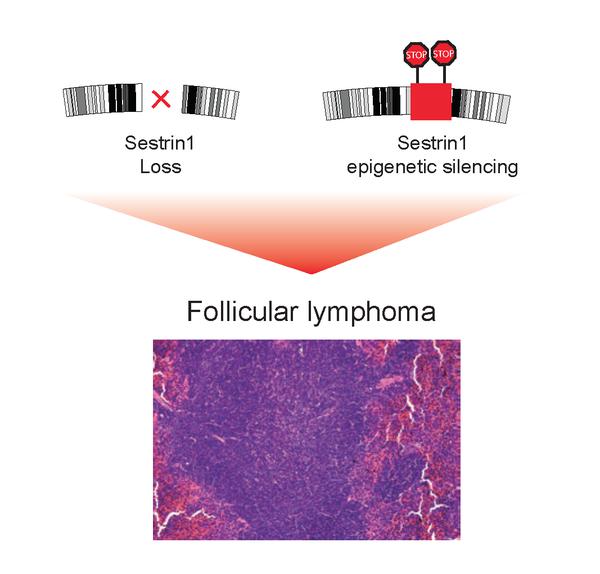
La désorganisation d'une région dans le chromosome 6, ou des modifications épigénétiques del'expression du bloc d'ADN Sestrine1, contribuent au développement du lymphome folliculaire.
Au-delà de l'identification du gène Sestrine1 comme étant fréquemment altéré chez les patients atteints de lymphome folliculaire, les scientifiques ont démontré que Sestrine1 est capable de détruire les tumeurs in vivo. Ils ont montré que Sestrine1 exerce ses effets anti-tumoraux en bloquant l'activité d'un complexe de protéines appelé mTORC1, bien connu pour contrôler la synthèse des protéines, tout en agissant comme un détecteur de changement nutritionnel ou énergétique dans la cellule.
En conclusion, l'identification de la perte de Sestrine1 comme événement-clé dans le développement du lymphome folliculaire est particulièrement importante, car elle aide à identifier les patients qui pourront bénéficier de nouvelles thérapies. De fait, cette étude montre que l'efficacité thérapeutique d'un nouveau médicament actuellement en cours d'essais cliniques dépend de Sestrine1. Il est à souligner que cette dépendance peut être étendue à d'autre types de tumeurs, au-delà du lymphome folliculaire.
Ce travail a été réalisé en collaboration avec le Memorial Sloan Kettering Cancer Center (New York), Cornell University, l'Université de Lausanne, Goodwin Research Laboratories, Trinity College Dublin, the BC Cancer Agency, the University of British Columbia, et the Princess Margaret Cancer Centre (Toronto).
Financement
Fonds National Suisse, Fondation ISREC, Fondation Giorgi-Cavaglieri, National Cancer Institute, Lymphoma Research Foundation, Mr. William H. Goodwin, Mrs. Alice Goodwin et la Commonwealth Foundation for Cancer Research, Memorial Sloan Kettering Cancer Center, National Institutes of Health, Starr Cancer Consortium, Geoffrey Beene Cancer Research Center, Leukemia and Lymphoma Society, et Princess Margaret Cancer Centre.
Référence
E. Oricchio, N. Katanayeva, M. C. Donaldson, S. Sungalee, P. P. Joyce, W. Béguelin, E. Battistello, V. R. Sanghvi, M. Jiang, Y. Jiang, M. Teater, A. Parmigiani, A. V. Budanov, F. C. Chan, S. P. Shah, R. Kridel, A. M. Melnick, G. Ciriello, H-G. Wendel. Genetic and epigenetic inactivation of SESTRIN1 controls mTORC1 and response to EZH2 inhibition in follicular lymphoma.Science Translational Medicine 9, eaak9969 (2017). DOI: 10.1126/scitranslmed.aak9969