Un «filet de sécurité» pour de nouvelles immunothérapies

Bruno Correia, Sailan Shui, Pablo Gainza, et Sandrine Georgeon© Alain Herzog / EPFL 2020
L’immunothérapie par cellules T CAR est extrêmement prometteuse pour le traitement de tumeurs, mais certains effets secondaires toxiques peuvent entraîner le décès des patients. Des chercheurs de l’EPFL, de l’UNIL et du CHUV ont mis au point un système pour désactiver la thérapie en cas de danger, et protéger les patients. Cette technique ouvre la voie à de nouvelles immunothérapies pour les cancers solides.
Depuis quelques années, l’immunothérapie obtient des résultats extraordinaires pour traiter des tumeurs dites liquides, telles que la leucémie et le lymphome. Au contraire de la chimiothérapie ou de la radiothérapie, l’immunothérapie stimule et arme notre propre système immunitaire, afin qu’il attaque les cellules cancéreuses.
L’une des approches, appelée CAR T-cell, consiste à extraire chez le patient les cellules les plus puissantes du système immunitaire – les cellules T -, et à les doter de récepteurs pour qu’elles détectent et détruisent les tumeurs. Dans le cas de tumeurs solides, cependant, les cellules T modifiées ont tendance à attaquer également des tissus sains, causant une haute toxicité, et des dommages importants sur les organes, menant même au décès du patient.
Pour contrôler ces effets secondaires, une équipe de chercheurs de l’EPFL, du Ludwig Institute for Cancer Research de l’UNIL et du CHUV, ont mis au point un système à base de protéines, qui permet «d’éteindre» l’activité des cellules T modifiées sur commande, en cas d’urgence. Ils créent ainsi un filet de sécurité pour le patient qui réagit mal à son traitement. Cette méthode de contrôle, appelée STOP-CAR, a été testée et validée sur des souris dotées du cancer de la prostate. Elle devrait permettre d’accélérer le développement clinique de nouvelles thérapies CAR, qui étaient jugées trop risquées jusqu’ici. La recherche est publiée dans Nature Biotechnology.
Médicaments vivants
Mais comment fonctionne ce système de sécurité ? La procédure de base est la même que pour les techniques actuelles. On extrait les cellules T du patient par simple prise de sang, puis on les transforme génétiquement, afin de faire croître des récepteurs – CARs- à leur surface. Ces récepteurs permettent à la cellule de reconnaître et de s’attacher à la surface des cellules tumorales. Une fois attachée, un signal est envoyé à l’intérieur de la cellule pour lui dire d’attaquer.
La nouveauté intervient à ce niveau. A l’aide de méthodes de design informatique de protéines, les chercheurs ont fabriqué un système qui, placé au niveau du récepteur, permet d’interrompre sur commande la transmission du signal à la cellule, après l’amarrage à un antigène tumoral. En interrompant cette connexion, la cellule T est inactivée.
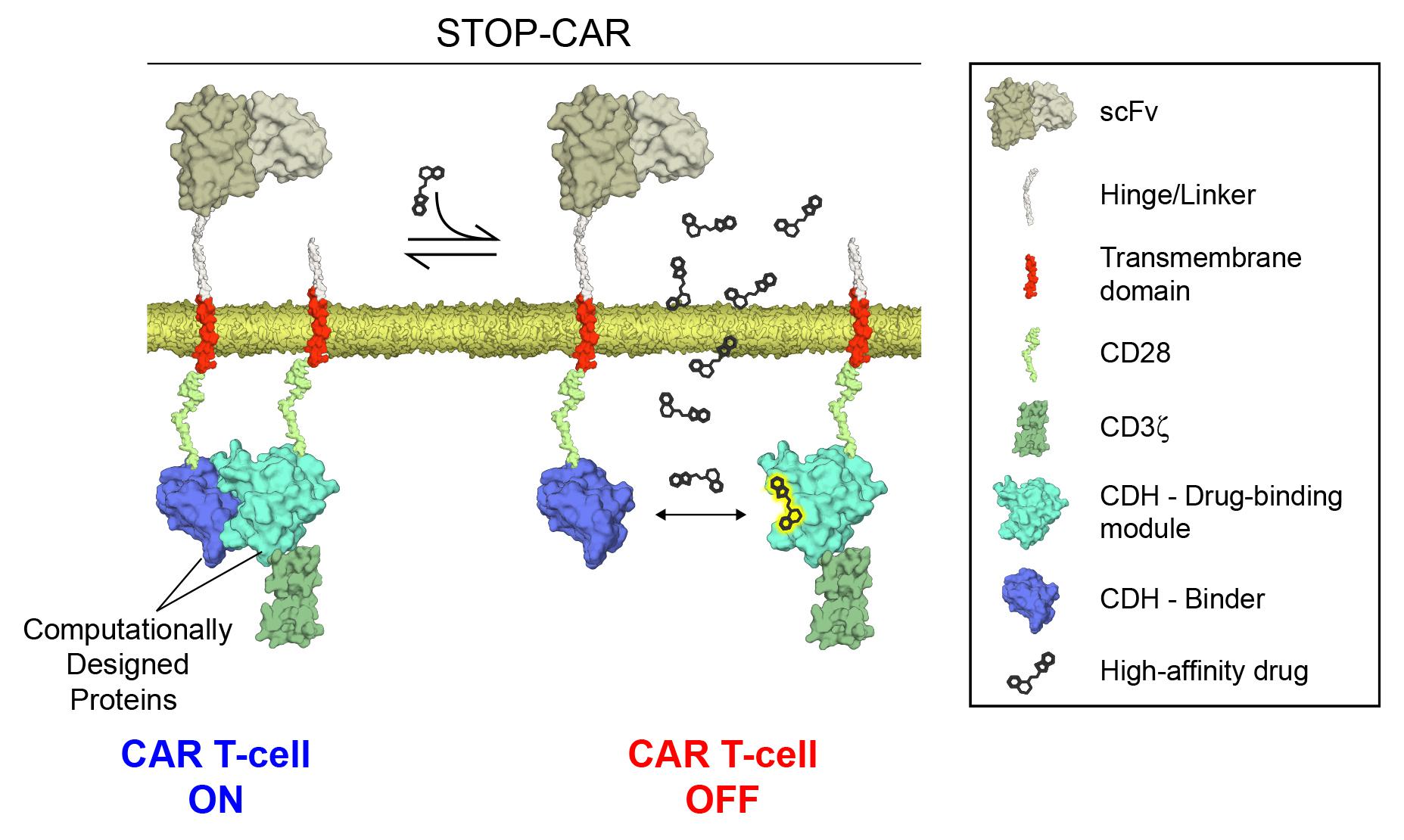
L’extinction de la cellule se fait par l’ajout d’une molécule, qui se traduit par une prise de médicament de la part du patient. Dans ce nouveau système, la cellule T est en effet dotée de paires de protéines naturellement liées, qui assurent la transmission de l’information entre le récepteur et l’intérieur de la cellule. Or si on leur ajoute une molécule spécifique, les protéines se délient, ce qui interrompt la communication, et éteint la cellule.
«Ce qui est intéressant, c’est qu’il nous est possible de réactiver la cellule T en arrêtant ce traitement», explique Bruno Correia, l’un des auteurs principaux de l’étude et professeur assistant à l’institut de bioingénierie de la faculté des Sciences et Techniques de l’Ingénieur de l’EPFL. «Nous n’avons pas besoin de détruire nos cellules T en cas de danger, et cela nous permet de contrôler parfaitement les effets de l’immunothérapie».
Autre atout, il a été observé que les cellules T ont tendance à s’épuiser si elles sont en contact avec les antigènes de manière prolongée. Cette méthode pourrait leur permettre de se reposer, avant de repartir au combat.
«Ce travail en soi, ainsi que son potentiel d’application, sont passionnants», déclare George Coukos, directeur de la branche du Ludwig Institute for Cancer Research, «il illustre également la façon dont des collaborations multidisciplinaires bien orchestrées peuvent donner lieu à des percées scientifiques importantes. En collaboration avec l'EPFL et nos autres partenaires de la région, nous espérons apporter la thérapie STOP-CAR-T le plus rapidement possible aux patients atteints de cancer.»
This study was supported by Ludwig Cancer Research, the Biltema and ISREC Foundations, the European Research Council, the National Center of Competence for Molecular Systems Engineering, The Marie Sklodowska-Curie Actions, Whitaker and the National Research Foundation of Korea.
G. Giordano-Attianese, P. Gainza, E. Gray-Gaillard, E. Cribioli, S. Shui, S. Kim, M.-J. Kwak, S. Vollers, A. De Jesus Corria Osorio, P. Reichenbach, J. Bonet, B.-H. Oh, M. Irving, G. Coukos, B. E. Correia, Computationally designed STOP-CAR disrupted by small molecule confers on-command regulation of T-cell therapy, Nature Biotechnology, DOI: 10.1038/s41587-019-0403-9