Des mitochondries saines, le meilleur atout contre Alzheimer
Mitochondries (iStock)
Par une approche à la fois bioinformatique et expérimentale, des chercheurs à l’EPFL ont découvert que des mitochondries rendues plus résistantes peuvent freiner les maladies causées par la toxicité amyloïde, telles que la maladie d’Alzheimer. L’étude est publiée dans Nature.
La maladie d’Alzheimer est la forme de démence et de neurodégénérescence la plus répandue dans le monde. L’une des caractéristiques majeures de la maladie est l’accumulation de plaques toxiques dans le cerveau, formées par l’agrégation anormale dans les neurones d’une protéine appelée béta-amyloïde.
Toujours sans remède, la maladie d’Alzheimer constitue une charge très lourde pour les systèmes publics de santé. La plupart des traitements actuels mettent l’accent sur la réduction de la formation de plaques amyloïdes, mais ces approches s’avèrent peu concluantes. De ce fait, les scientifiques cherchent aujourd’hui des stratégies de traitements alternatifs, parmi lesquelles celle de considérer la maladie d’Alzheimer en tant que maladie métabolique.
Dans le prolongement de cette idée, le laboratoire de Johan Auwerx à l’EPFL s’est penché sur les mitochondries, de véritables centrales énergétiques qui se trouvent dans chaque cellule, et sont donc au cœur du métabolisme cellulaire. En prenant comme modèles d’études des vers et des souris, ils ont découvert qu’une stimulation des défenses des mitochondries contre une forme particulière de stress des protéines conduisait à une réduction de la formation de plaques amyloïdes.
Durant le vieillissement normal ou lors de maladies associées au vieillissement telles qu’Alzheimer, les cellules sont sans cesse confrontées à une augmentation de lésions et doivent donc constamment se battre pour protéger et remplacer des mitochondries dysfonctionnelles. Les mitochondries fournissent de l’énergie aux cellules du cerveau ; chez un patient souffrant de la maladie d’Alzheimer, si elles ne sont pas protégées, cela favorise des lésions au niveau du cerveau, donnant ainsi lieu, au cours des années, aux symptômes caractéristiques de la maladie dont la perte de mémoire.
Les scientifiques ont identifié deux mécanismes qui contrôlent la qualité des mitochondries. D’une part la « mitochondrial unfolded protein response » (UPRmt), une réaction qui protège les mitochondries du stress cellulaire. D’autre part, la mitophagie, un processus responsable du recyclage des mitochondries défectueuses. Ces deux mécanismes sont essentiels pour retarder ou prévenir trop de lésions mitochondriales chez un malade.
Alors que nous savons depuis quelque temps que les mitochondries sont dysfonctionnelles dans le cerveau de patients souffrant de la maladie d’Alzheimer, ceci constitue la première preuve que ces organelles tentent bel et bien de combattre la maladie en stimulant des voies de contrôle de qualité. « Ces voies de défense et de recyclage des mitochondries sont essentielles et existent chez tous les organismes, du ver C. elegans jusqu’aux êtres humains, » dit Vincenzo Sorrentino, auteur principal de l’article. « C’est pourquoi nous avons décidé de les activer de manière pharmacologique. »
L’équipe a commencé par mettre à l’essai des composés – tels que l’antibiotique doxycycline ou la vitamine nicotinamide riboside (NR) – capables d’enclencher les systèmes de défense UPRmt et mitophagiques chez le ver (C. elegans), un organisme modèle pour les travaux sur la maladie d’Alzheimer. Lors de comparaison avec des vers non traités, les scientifiques ont remarqué que la santé, l’activité et la longévité des vers exposés aux médicaments avaient augmenté de manière remarquable. La formation des plaques s’est aussi considérablement réduite chez les animaux traités.
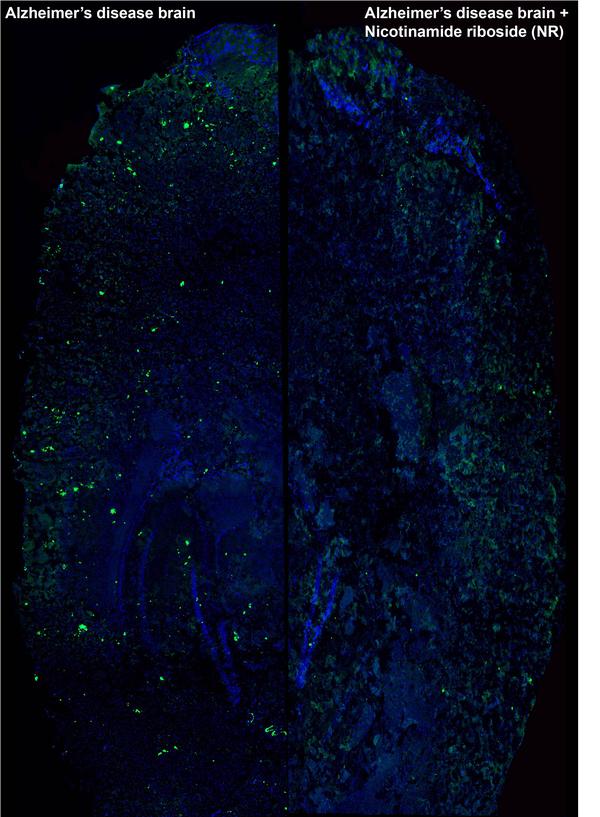
Coupes de l'hémisphère cérébral de souris Alzheimer, modèle APP / PSEN1, avant et après traitement avec le rappel NAD + Nicotinamide riboside (NR). La teneur en plaques bêta-amyloïdes dans le cerveau des souris APP / PSEN1 (à gauche), clairement visible par coloration à la thioflavine S de couleur verte et associée à des lésions cérébrales pendant la maladie, est réduite après 10 semaines de traitement par NR (droite). Crédit: Vincenzo Sorrentino, Mario Romani, Francesca Potenza / EPFL.
Plus important encore, les chercheurs ont observé des améliorations similaires en enclenchant les mêmes voies de défense mitochondriales au sein de cellules neuronales humaines cultivées.
Ces résultats encourageants les ont alors incités à tester la nicotinamide chez la souris, autre organisme modèle pour la maladie d’Alzheimer. Tout comme pour C. elegans, la fonction mitochondriale chez la souris s’est améliorée de manière significative et les scientifiques ont pu observer une réduction du nombre de plaques amyloïdes. Mais surtout, ils ont relevé une surprenante normalisation de la fonction cognitive des souris – ce qui, d’un point de vue clinique, a des implications extrêmement importantes.
Selon Johan Auwerx, s’atteler à la maladie d’Alzheimer par le biais des mitochondries pourrait faire toute la différence. « Jusqu’à présent, la maladie d’Alzheimer a été considérée comme étant due essentiellement à l’accumulation de plaques amyloïdes dans le cerveau, » explique-t-il. « Nous avons démontré qu’en restaurant la santé mitochondriale, la formation des plaques est réduite – mais, avant tout, cette santé mitochondriale améliore la fonction du cerveau, ce qui est tout de même l’objectif ultime des chercheurs comme des patients souffrant de la maladie. »
La stratégie offre une nouvelle approche thérapeutique pour ralentir la progression de la neurodégénérescence dans la maladie d’Alzheimer, et peut-être même la progression d’autres affections telles que la maladie de Parkinson – caractérisée elle aussi par de très grandes anomalies mitochondriales et métaboliques.
L’approche doit encore être testée chez les humains. « En ciblant les mitochondries, des molécules telles que la nicotinamide riboside qui savent stimuler les systèmes de ‘défense et de recyclage’ de ces organelles pourraient réussir là où tant de médicaments – dont la grande majorité cherche à diminuer la formation de plaques amyloïdes – ont échoué, » poursuit Vincenzo Sorrentino.
Contributeurs
- Michigan State University
- EPFL Proteomics Core Facility
Financement
- ‘EPFL Fellows’ program (co-funded by the Marie Skłodowska-Curie, Horizon 2020 Grant)
- Associazione Italiana per la Ricerca sul Cancro (AIRC)
- National Institutes of Health (NIH)
- Systems X
- Velux Stiftung
- The Jebsen Foundation
- Swiss National Science Foundation
Réference
Vincenzo Sorrentino, Mario Romani, Laurent Mouchiroud, John S. Beck, Hongbo Zhang, Davide D’ Amico, Norman Moullan, Francesca Potenza, Adrien W. Schmid, Solène Rietsch, Scott E. Counts, Johan Auwerx. Enhancing mitochondrial proteostasis reduces amyloid-β proteotoxicity. Nature 06 December 2017. DOI: 10.1038/nature25143