Un contrôle médical complet sur puce

© 2014 EPFL
De la taille d'une agrafeuse, un nouveau dispositif portable développé à l'EPFL permet de tester simultanément une foule de protéines présentes dans notre corps. Cet outil de diagnostic combine un subtil mélange d'optique et d'ingénierie.
Sera-t-il un jour possible d'effectuer un bilan de santé sans passer par la case médecin? La dernière trouvaille de l'EPFL va en tous cas dans ce sens. La Professeure Hatice Altug et son postdoctorant Arif Cetin, en collaboration avec le professeur Aydogan Ozcan de l'UCLA, ont développé un «laboratoire sur puce» optique compact et peu cher, capable d'analyser rapidement jusqu'à 170'000 molécules différentes dans un échantillon sanguin. Le taux d'insuline, les marqueurs de cancers, d'Alzheimer ou encore certains virus pourraient ainsi être identifiés de manière simultanée. «Nous voulions construire une interface qui, à l'image du tableau de bord d'une voiture, peut donner des indications tant sur le niveau d'essence et d'huile, que sur l'état des phares ou du moteur», explique la chercheuse.
Traditionnellement, pour effectuer une analyse, on observe les changements de spectre de la lumière qui traverse un échantillon. Dans cette étude, les chercheurs s'intéressent au contraire à l'intensité de la lumière, ce qui permet de se débarrasser des spectromètres encombrants.
Une précision de quelques nanomètres
Haut de 7,5cm, le dispositif de 60 grammes est capable de détecter des monocouches de protéines épaisses de 3 nanomètres, ainsi que des virus. Il fait l'objet d'une publication dans Nature Light Science & Application. La recette est simple et se résume à quelques ingrédients : Une puce CMOS, une diode électroluminescente (LED) et une plaquette en or de 10x10millimètres, dotée de minuscules trous de moins de 200 nanomètres de large.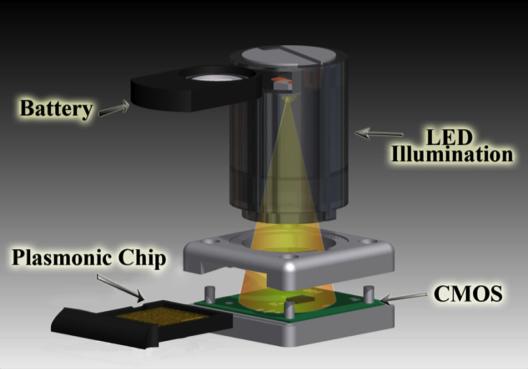
Sur la plaquette en or, les nano-trous sont répartis par section. Chacune de ces sections fonctionnant comme un capteur indépendant. Doté d'un biofilm spécial, chaque capteur peut ensuitec retenir différents types de protéines. Ainsi, lorsque l'échantillon à analyser est versé sur la plaquette, les protéines sont « capturées » au à différents endroits sur la plateforme, et peuvent être analysées simultanément.
L'intensité de la lumière passée au crible
La détection des protéines piégées se fait presque immédiatement, grâce à l'entrée en scène de la diode. La lumière éclaire la plateforme, passe par les nano-ouvertures, et ses propriétés sont enregistrées par la puce CMOS. Comme les particules changent les propriétés de la lumière, il est possible de déduire le nombre de particules accrochées aux capteurs.
Habituellement, on regarde la différence de longueur d'onde de la lumière au départ et à l'arrivée. Seul hic : cette technique requiert la présence d'appareils volumineux comme les spectromètres. L'astuce d'Hatice Altug consiste à se focaliser non pas sur les différences de longueur d'onde - ou de spectre-, mais sur les différences d'intensité de la lumière. Cette façon de faire est possible grâce à un phénomène physique appelé « résonance des plasmons de surface ». En résumé, sous l'effet de la lumière, les électrons situés au bord des trous se mettent à osciller de manière collective. Or cette oscillation est différente selon qu'une protéine est présente ou non. La puce CMOS n'aura plus qu'à enregistrer et mesurer l'intensité de l'oscillation.
Modeler le dispositif à sa guise
La taille, le coût et l'efficacité de ce nouveau dispositif multi-analyses en fait un instrument hautement prometteur. «Des études récentes ont démontré que pour certaines maladies comme les cancers ou Alzheimer, le fait de pouvoir analyser plusieurs paramètres à la fois permet de poser un meilleur diagnostique et d'éviter les résultats faussement positifs», commente Hatice Altug. «Il est par ailleurs possible de retirer la plaquette de l'appareil et de la réinsérer, ce qui nous permet de l'adapter à un grand nombre recherches biomédicales et environnementales», poursuit-elle. L'équipe de la chercheuse va maintenant tenter de collaborer avec les hôpitaux de la région, afin de trouver le meilleur moyen d'utiliser cette technologie.
Plus d'informations : Handheld high-throughput plasmonic biosensor using computational on-chip imaging