Des chambres d'observation pour comprendre le langage des cellules
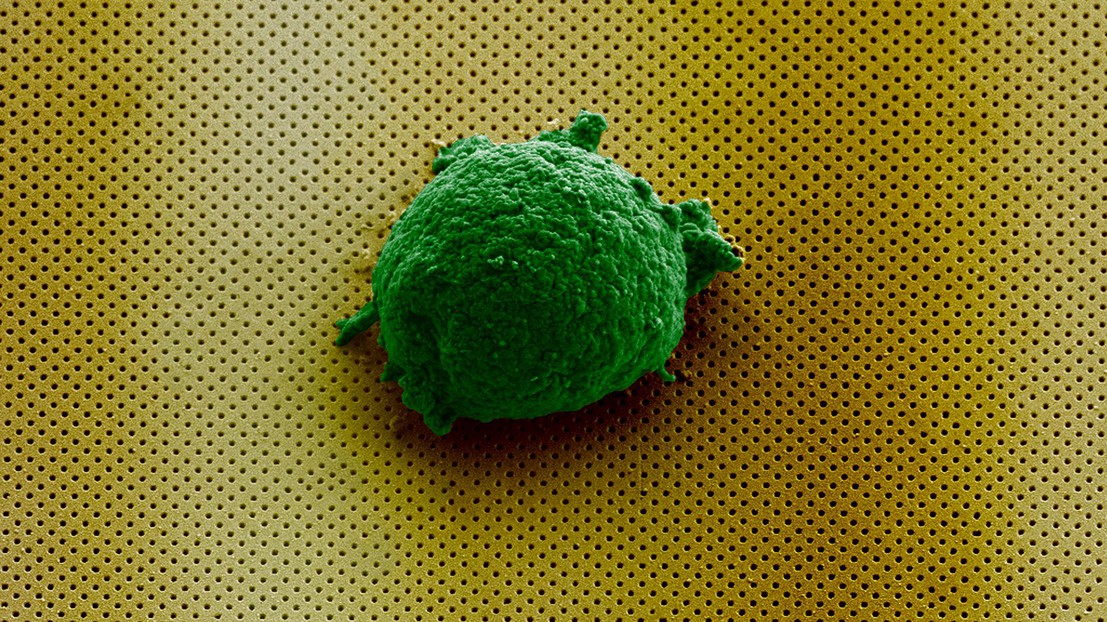
Image microscopique d'une cellule artificiellement colorée, reposant sur des milliards de nanopores© A paraître sur la couverture de la revue Small / 2018 EPFL
Des chercheurs de l’EPFL ont créé un appareil inédit pour étudier en temps réel et en continu le comportement individuel des cellules vivantes. Chaque sujet est placé dans un compartiment, puis observé durant son cycle de vie tout entier. Cette plateforme permet de cerner la personnalité des cellules et de comprendre leur langage. Elle constitue un outil puissant pour sélectionner les sujets les plus combatifs face à un ennemi. A la clé, la création de nouveaux traitements en cas de cancers ou de maladies auto-immunes.
A l’image des êtres humains, les cellules d’une même espèce disposent toutes d’une «personnalité» bien distincte. Confrontées à un stimulus externe, tel qu’un virus, elles sécréteront chacune une quantité différente de molécules et communiqueront avec leur congénères de façon plus ou moins intense. La littérature scientifique a déjà démontré que deux cellules de même type soumises à un même traitement réagissaient de façons diverses.
Pour étudier ce phénomène, des scientifiques de l’EPFL ont fabriqué un outil inédit, en collaboration avec l’Université RMIT en Australie, et l’Université de Lausanne. Il s’agit d’un dispositif optofluidique doté d’une chambre mille fois plus petite qu’une goutte de pluie. A l’intérieur, une cellule peut être déposée, puis observée en temps réel, sans perturber son environnement. La quantité et le type de sécrétions de la cellule sont identifiés en continu. Compatible avec les microscopes traditionnels, la plateforme a déjà fonctionné pendant 12 heures, et pourrait tenir bien plus longtemps. Elle constitue un outil de sélection puissant et inédit. Les résultats sont publiés dans la revue scientifique Small.
Etudier les cellules une à une
Le fonctionnement de chaque cellule du corps humain est complexe. Pour proliférer, et envahir des tissus sains, les cellules cancéreuses produisent différentes hormones et protéines. De même, face à une infection ou un ennemi, les cellules immunitaires sécrètent des médiateurs chimiques appelés cytokine, qui stimulent le système immunitaire pour détruire l’intrus. Mais comment chacune de ces cellules réagit-elle très précisément ?
Il existe de nombreuses études sur le comportement des cellules en groupe, mais on manque encore d’informations sur leur fonctionnement individuel. Le nouvel outil proposé par les chercheurs, léger et transportable, constitue une nouvelle clé de compréhension du fonctionnement de chaque cellule, et de leur manière de communiquer. Il ouvre la voie à la création de nouvelles thérapies en cas de cancer, ou pour traiter des maladies auto-immunes. « On pourrait par exemple sélectionner les cellules immunitaires les plus efficaces, pour combattre la maladie », explique Hatice Altug, co-auteure de l’étude et directrice du Laboratoire de systèmes bionanophotoniques – Faculté des sciences et techniques de l’ingénieur- EPFL.
Une seule cellule nourrie, logée et scrutée
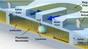
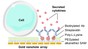
Le bio-capteur nanophotonique imaginé par les chercheurs prend la forme d’une petite chambre chauffée, dont les parois sont constituées de membranes poreuses. Elle est alimentée en continu en eau et en nutriments par de minuscules canaux microfluidiques. La température et le taux d’humidité sont strictement contrôlés. A l’aide de valves, une cellule peut être introduite dans un compartiment. Le sol de la chambre est recouvert d’un mince film d’or percé de milliards de nanopores, arrangés selon un schéma précis. Des ligands ou anticorps sont placés autour des nanopores. Ils ont pour mission de reconnaître et d’accrocher les molécules spécifiques qui seront sécrétées par la cellule.
Une lumière à large bande est envoyée en continu sur le compartiment. Par un phénomène optique unique appelé plasmons, les nanopores ne laissent passer qu’une seule fréquence ou couleur. Lorsqu’une molécule est sécrétée par la cellule, elle s’accroche aux anticorps, et la fréquence transmise par les nanopores en est modifiée. Cela permet de détecter la présence d’infimes quantités de molécules.
Les scientifiques ont déjà pu étudier les différents niveaux de sécrétion de cytocine chez une cellule de type lymphome.
«Jusqu’ici, les méthodes pour étudier les cellules individuellement ont toujours impliqué l’utilisation de fluorophores, ce qui perturbe le fonctionnement de la cellule, et empêche leur étude sur de longues périodes», indique Hatice Altug. «Dans notre dispositif, chaque nanopore constitue un capteur en soi. La cellule peut donc s’installer naturellement n’importe où dans la chambre, et nous pourrons l’analyser de la même façon», ajoute Maria Soler, co-premier auteur de l’étude.
Les applications sont légions. «Lors d’une tumeur, on pourrait imaginer identifier les cellules cancéreuses les plus agressives, afin de savoir précisément quel traitement administrer au patient», évoque Xiaokang Li, premier auteur de l’étude.
Partenaires:
Laboratoire de systèmes bionanophotoniques / EPFL
Integrated Photonics and Application Center / Université RMIT
Ludwig Institute for Cancer Research Lausanne / Université de Lausanne
Référence : X. Li, M. Soler, C. Szydzik, K. Khoshmanesh, J. Schmidt, G. Coukos, A. Mitchell and H. Altug, Label-Free Optofluidic Nanobiosensor Enables Real-Time Analysis of Single-Cell Cytokine Secretion, Small