De la 3d multicolore grâce à la microscopie à super-résolution
© 2018 EPFL
Une nouvelle technique développée par l'EPFL surmonte le problème du bruit et des limitations de la couleur dans la microscopie à super-résolution, en créant des reconstructions tridimensionnelles (3D) de complexes de protéines à partir d'image à deux dimensions en couleur unique (2D).
La microscopie à super-résolution est une technique capable de «voir» au-delà de la limite de diffraction de la lumière. Cette technique a récemment bénéficié d'un intérêt croissant, en particulier depuis que ses développeurs ont gagné le Prix Nobel de Chimie en 2014. En exploitant la fluorescence, la microscopie à super-résolution permet désormais aux scientifiques d'observer des cellules, leurs structures internes et leurs organelles d'une manière qui n'avait jamais été possible jusqu'ici.
À l'intérieur des cellules, nombre de complexes moléculaires sont constitués de multiples protéines. Dans la mesure où les techniques courantes de microscopie à super-résolution ne peuvent utiliser typiquement qu'une ou deux couleurs fluorescentes, il est difficile d'observer différentes protéines et de déchiffrer l'architecture complexe et les mécanismes d'assemblage sous-jacents des structures internes de la cellule. Un défi encore plus grand est de surmonter le bruit inhérent aux méthodes de super-résolution et au marquage fluorescent pour parvenir au potentiel de pleine résolution.
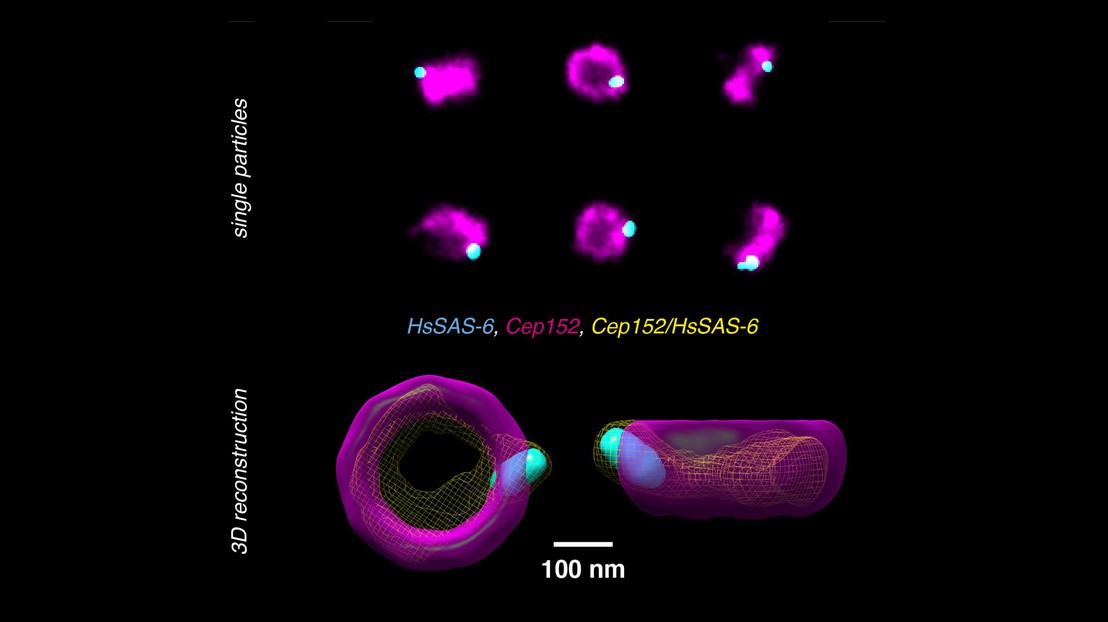
Des scientifiques du laboratoire de Suliana Manley à l'EPFL viennent de résoudre les deux problèmes en développant une nouvelle méthode pour analyser et reconstruire des images en super-résolution, et les réaligner d'une telle manière que les multiples protéines puissent être placées à l'intérieur d'un volume 3D unique. La méthode fonctionne avec des images prises au moyen de la microscopie à super-résolution à grand-angle, chaque image contenant des centaines de projections en deux dimensions d'une structure marquée en parallèle. Chaque image 2D représente une orientation légèrement différente de la structure, de sorte qu'avec une base de données de milliers de vues, la méthode peut, au moyen de l'informatique, reconstruire et aligner les images 2D en un volume 3D. En combinant les informations d'un nombre plus grand d'images uniques, le bruit diminue et la résolution effective de la reconstruction 3D est améliorée.
Avec l'aide du laboratoire de Pierre Gönczy à l'EPFL, les chercheurs ont testé la méthode sur des complexes de centrioles humains. Les centrioles sont des paires d'ensembles moléculaires cylindriques qui sont essentielles pour aider la cellule à se diviser. En utilisant la nouvelle méthode de reconstruction en super-résolution multicolore, les chercheurs ont pu découvrir l'architecture 3D de quatre protéines nécessaires à l'assemblage centriolaire pendant la biogenèse des organelles.
La nouvelle approche autorise des capacités de multiplexage illimitées. «Avec cette méthode, pour peu que les protéines à l'intérieur de la structure puissent être marquées, il n'y a pas de limites au nombre de couleurs de la reconstruction 3D, dit Suliana Manley. De plus, la reconstruction est indépendante de la méthode de super-résolution utilisée, et nous pensons donc que cette méthode d'analyse et son logiciel présentent un grand intérêt.»
Conseil européen de la recherche
EPFL
Horizon 2020 (MSCA-COFUND)
NCCR Chemical Biology
Christian Sieben, Niccolò Banterle, Kyle M. Douglass, Pierre Gönczy, Suliana Manley. Multicolor single particle reconstruction of protein complexes. 01 October 2018. DOI: 10.1038/s41592-018-0140-x